Учреждение разработчик:
ГУЗ «Московский научно-практический центр оториноларингологии » Департамента здравоохранения города Москвы.
Составители:
- доктор мед. наук, профессор А.И. Крюков
- доктор мед. наук, профессор Н.Л. Кунельская
- кандидат мед. наук, руководитель отделения патологии
- верхних дыхательных путей А.Б. Туровский
- кандидат мед. наук Д.В. Кравченко
Рецензенты:
Зав. кафедрой оториноларингологии РУДН, профессор В.Ф.Антонив
Профессор кафедры болезней уха, горла и носа МММ им. И.М.Сеченова В.П.Гамов
Предназначение:
Методические рекомендации содержат лечебно-диагностический алгоритм при орбитальных риносинусогенных осложнениях. Рекомендации предназначены для врачей-оториноларингологов и офтальмологов..
Данный документ является собственностью Департамента Здравоохранения города Москвы и не подлежит тиражированию и распространению без соответствующего разрешения.
Список сокращений
- ГБО — гипербарическая оксигенация.
- КТ – компьютерное томографическое исследование.
- МРТ – магнитно-резонансное томографическое исследование
- ОГС – острый гнойный синусит.
- ОРО – орбитальные риносинусогенные осложнения.
- РНЭТ — регионарная непрямая эндолимфатическая терапия.
- ТАМЭ – транспортная активность мерцательного эпителия.
- ФЭРСХ — функциональная эндоскопическая риносинусохирургия.
- ХГС – хронический гнойный синусит.
- ЭИ – эндоскопическое исследование.
Введение
Параназальный синусит, в особенности гнойные его формы, являются наиболее частой причиной орбитальных воспалительных осложнений, по наблюдениям ряда авторов от 0,5% до 8,4% случаев, представляющих опасность как для зрения, так и для жизни больного. Однако к настоящему моменту времени причины возникновения указанной патологии орбиты, с появлением КТ и ЭИ, требуют уточнения.
Вопросам диагностики и лечения орбитальных риносинусогенных осложнений посвящено большое число научных трудов как оториноларингологов, так и офтальмологов. Улучшение общего состояния больного было главной задачей. Смертность от данного заболевания в настоящее время сведена к минимуму благодаря применению антибиотиков и разработанных методов хирургического лечения гнойных синуситов. Но прогноз в плане зрения остается неблагоприятным и связан с нарушением кровообращения зрительного нерва. Согласно данным различных исследований, слепота наступает у 0,8 — 3% больных с риносинусогенным орбитальным осложнением.
Поэтому проблема повышения эффективности диагностики и лечения ОРО остается актуальной и современной.
Этиологические предпосылки возникновения орбитальных
риносинусогенных осложнений.
Традиционно считается, что этиологическим фактором возникновения ОРО являются те же возбудители, что и при синусите, который вызвал данное осложнение. Как правило, основными возбудителями ОГС являются Streptococcus pneumoniae, Haemophillus influenzae и Moraxella catarrhalis, анаэробные микроорганизмы. При ХГС возрастает удельный вес грамотрицательной микрофлоры, анаэробной микрофлоры (40%). Среди штаммов, высеваемых из отделяемого, полученного из околоносовых пазух при хроническом воспалении, наиболее часто определяются: Staphylococcus aureus (18,4%), Pseudomonas aeruginosae (5%), Escherichia colli (4,5%), Haemophilus influenzae (4,5%), Streptococcus pneumoniae (3,9%), Enterobacter aerogenes (3,4%), Moraxella catarrhalis (2,8%). Значительно реже встречаются Serratia marcenscans, Klebsiella species, Proteus mirabilis, Citrobacter, Streptococcus agalactiae, α-hemolytic Streptococcus, β- hemolytic Streptococcus.
В настоящее время отмечается рост устойчивости пневмококка к таким лекарственным препаратам, как полусинтетические пенициллины и макролиды. Практически не встречается штаммов, устойчивых к аминопенициллинам (амоксициллин) и фторхинолонам последнего поколения (левофлоксацин и моксифлоксацин).
Отмечается рост резистентности к пенициллинам многих штаммов Haemophillus influenzae, что связано с выработкой ими беталактамаз. В России частота встречаемости пенициллиназообразующих штаммов не превышает 14%. Высокая активность в отношении H. influenzae наблюдается среди аминопенициллинов, потенцированные против β-лактамаз клавулановой кислотой (амоксициллин-клавуланат, ампициллин – сульбактам, тикарциллин – клавуланат); цефалоспоринов (цефуроксим, цефтриаксон) и фторхинолоны (левофлоксацин, моксифлоксацин).
Штаммы M. catarrhalis (до 98%) продуцируют β-лактамазы, в связи с чем являются нечувствительными к действию незащищенных аминопенициллинов.Они сохраняют высокую чувствительность к защищенным аминопенициллинам (амоксициллин-клавуланат), цефалоспоринам, макролидам (азитромицин. кларитромицин) и фторхинолонам (левофлоксацин, моксифлоксацин).
По данным наших исследований при воспалительном процессе в орбите наиболее часто отмечаются S. aureus, стрептококки группы A, энтеробактерии, H. Influenzae. Наряду с этим, в ряде случаев определяются бактерии кишечной группы (энтерококки, кишечная палочка, протей). Практически во всех случаях отмечается смешанная флора (аэробная и анаэробная), среди последней встречаются представители Peptostreptococcus spp., Prevotella spp., Bacteroides spp., Peptococcus spp., Veillonella spp., Prevotella spp., Fusobacterium spp., Corynebacterium spp. совместно с Staphylococcus aureus, продуцирующими β-лактамазу стрептококками.
Анатомические предпосылки возникновения орбитальных
риносинусогенных осложнений
Возможность возникновения ОРО обусловлена анатомическими особенностями расположения и строения орбиты. Костная основа орбиты имеет форму четырехсторонней пирамиды, которую составляют семь отдельных костей. Верхняя стенка соприкасается с дном лобной пазухи, нижняя является крышей верхнечелюстной, медиальная стенка состоит из очень тонкой папиросной пластинки решетчатого лабиринта и соприкасается с клиновидной пазухой. Стенки орбиты покрыты периостом, который рыхло соединен с подлежащими костями, за исключением зоны швов. Данная особенность строения способствует легкой отслойке периоста при распространении инфекции контактным путем. Тарзорбитальная фасция отделяет содержимое орбиты от мягких тканей век, выполняя роль дополнительной стенки, перед ней в начальном отделе орбиты расположены веки и слезный мешок, глазное яблоко и окончания мышц. Кзади от глазничной перегородки находится зрительный нерв, глазодвигательные мышцы, нервно-сосудистые образования орбиты и жировая клетчатка.
В патогенезе орбитальных осложнений при синуситах важны и следующие анатомические факторы: 1) верхняя и нижняя стенка орбиты являются стенками лобной и верхнечелюстной пазух, 2) медиальная стенка орбиты граничит с клетками решетчатой пазухи и имеет 3 щели (слезно-верхнече-люстную, слезно-решетчатую и клиновидно-решетчатую), 3) венозная и лимфатическая системы орбиты тесно связаны с таковыми носа и околоносовых пазух, 4) периост орбиты наиболее слабое место при распространении инфекции из пазух носа, так как содержимое орбиты отделено барьером только из мягких тканей.
Одним из вариантов строения орбиты является наличие дегисценций в области между верхней и медиальной стенками орбиты, что приводит к соприкосновению слизистой оболочки клеток решетчатого лабиринта и содержимого орбиты.
Распространение патологического процесса из околоносовых пазух происходит чаще всего гематогенно, контактно — через дегисценции папиросной пластинки или через разрушенную гнойно — воспалительным процессом кость, периневрально, а также лимфогенно.
Инфицирование глазницы гематогенным путем происходит через мелкие венозные сосуды решетчатого лабиринта, которые прободают костную стенку глазницы и через венозные ветви, впадающие в верхнюю глазничную вену. Лимфогенный путь распространения инфекции играет важную роль при ОРО, несмотря на отсутствие лимфатических узлов и сосудов в орбите. Основной ток лимфы происходит по периваскулярным пространствам и через нижнюю глазничную щель в крылонебную ямку.
По нашим наблюдениям, в большинстве случаев причиной ОРО являются воспалительные процессы в решетчатом лабиринте, которые встречали в 100 (41,5%) случаях. Вовлечение в воспалительный процесс верхнечелюстной пазухи наблюдали в 70 (29%) случаях, лобной в 50 (20,7%), в клиновидной пазухе в 21 (8,7%).
Таким образом, патогенез ОРО при синуситах — прямой контакт с инфекционным агентом (часто при врожденных дефектах стенок орбиты), бактериальный флебит или проникновение бактерий по периваскулярным путям.
Классификация ОРО.
Б.В. Шеврыгин и Н.И. Куранов в 1976 г. предложили классификацию, в которую вошли: 1) реактивный отек клетчатки глазницы и век; 2) диффузное негнойное воспаление клетчатки глазницы и век; 3) периостит орбиты; 4) субпериостальный абсцесс; 5) абсцесс века; 6) свищи века и глазничной стенки; 7) ретробульбарный абсцесс; 8) флегмона орбиты; 9) тромбоз вен глазничной клетчатки. Данная классификация является наиболее полной и позволяет более тщательно вести разработку статистических материалов об ОРО и учет отдаленных результатов.
Нами наблюдались различные формы ОРО. Так, реактивный отек век был выявлен в 16 (14%) случаях, реактивный отек век с орбитальным отеком в 22 (19,3%) случаях, серозное (негнойное) воспаление орбитальной клетчатки (орбитальный целлюлит) отмечали у 13 (11,4%) больных. Преобладали гнойные воспалительные процессы в орбите как при острых (25 (54,3%), так и при хронических гнойных синуситах (38 (55,9%). Наиболее часто встречали среди гнойных осложнений субпериостальные и орбитальные (ретробульбарные) абсцессы (в 25 (21,9%) и 19 (16,7%) случаях соответственно). Орбитальная флегмона была выявлена в 12 (10,5%) случаях, абсцесс века в 7 (6,1%) случаях.
Клиническая симптоматика
Клиническая симптоматика ОРО складывается из проявлений гнойного воспалительного процесса в околоносовых пазухах и воспаления со стороны орбиты. К общим симптомам относят слабость, головную боль, общее недомогание, субфебрильную или фебрильную температуру тела.
Со стороны полости носа и околоносовых пазух наблюдается, как правило, затруднение носового дыхания, ощущение заложенности носа, отсутствие обоняния, выделения из носа гнойного или слизисто-гнойного характера. Наряду с данными симптомами отмечают головную боль, ощущение тяжести или давления в проекции пораженной пазухи.
Согласно данным оториноларингологического исследования у больных с ОРО отмечается болезненность при перкуссии мест проекций околоносовых пазух, болезненность точек выхода тройничного нерва. Основным патогномоничным признаком гнойного синусита, вызвавшего ОРО, является полоска гнойного или слизисто-гнойного отделяемого под средней носовой раковиной, однако данный симптом в 36,1% случаев может отсутствовать за счет нарушения проходимости соустья вовлеченной в гнойно-воспалительный процесс околоносовой пазухи. Отек и гиперемия слизистой оболочки полости носа встречаются и при других воспалительных заболеваниях, поэтому их нельзя считать достоверными симптомами параназального синусита.
Признаками ранней воспалительной реакции со стороны орбиты являются отек и гиперемия век, боль в глазу, гнойные выделение из носа и повышение температуры тела. Если воспалительный процесс продолжает развиваться дальше, то появляются птоз, экзофтальм, хемоз и ограничение подвижности глазного яблока вплоть до полной офтальмоплегии, что является признаками гнойного процесса в ретробульбарной области (абсцесса или флегмоны орбиты). Эти признаки говорят уже о воспалении мягких тканей и возможном тромбозе вен орбиты. Дальнейшее течение воспаления приводит к тромбозу кавернозного синуса, который характеризуется довольно быстрым распространением воспаления на другой глаз, внутричерепным осложнениям (менингит, абсцесс мозга), нарушению зрения — диплопии, снижению остроты зрения, слепоте.
Экзофтальм, как симптом заболевания орбиты, встречается при воспалении, травме, опухолях и может быть первым клиническим признаком протекающего ОРО. Хемоз, как правило, характерен для гнойных воспалительных процессов в орбите как пресептальных по отношению к тарзоорбитальной фасции, так и постептальной локализации.
Расположение гнойного очага в передних клетках решетчатого лабиринта сопровождается отеком внутреннего угла глаза, дакриоциститом, хемозом внутренней половины конъюнктивы глазного яблока. В случае наличия гнойного очага в задних клетках решетчатого лабиринта и клиновидной пазухе характерны центральная скотома, параличи III, IV и VI пар черепно-мозговых нервов, увеличение слепого пятна.
Воспалительный процесс в тканях орбиты приводит к повышению орбитального тонуса, что нарушает физиологический дренаж жидкости в венулах и капиллярах, вследствие этого повышается гидростатическое давление, что вызывает венозный застой в глазном яблоке и как результат возникает псевдоотек диска зрительного нерва.
Чем ближе фокус воспаления к глазному яблоку, тем выше вероятность появления офтальмологической картины. В связи с этим на глазном дне появляются: отек, гиперемия зрительного нерва, геморрагии, изменения калибра сосудов. Воспаление и отек зрительного нерва приводят к его сдавлению в костном канале, диаметр которого составляет 4 — 5 мм, а сам нерв без оболочек – 3 мм.
Наиболее опасно попадание в центр воспалительного процесса зрительного нерва и основных сосудов. Этим обстоятельством объясняется более частое появление слепоты при флегмоне, чем при абсцессе орбиты.
Из орбитальных осложнений воспалительных заболеваний околоносовых пазух более частыми и лучше изученными являются заболевания стенок глазницы и ретробульбарной клетчатки, тогда как поражение глазного яблока и зрительного нерва наблюдается реже. Из заболеваний глазного яблока, прежде всего, заслуживает внимания повреждение соединительнотканной и роговой оболочек.
Панофтальмит — воспаление всех тканей и оболочек глаза — возникает чаще в результате экзогенного попадания инфекции при ранении глазного яблока, однако возможен и метастатический занос инфекции. Первичный очаг воспаления при этом может локализоваться не только в отдаленных органах, но и по соседству, в частности околоносовых пазухах. Тяжелые случаи панофтальмита приводят к атрофии глазного яблока и, естественно, к полной потере зрения на этот глаз. Кроме того, панофтальмит опасен возможностью развития внутричерепных осложнений с летальным исходом при распространении инфекции по сосудам в кавернозный синус. В случае выздоровления остается парез III, IV и VI пар черепномозговых нервов.
Диагностические методы при ОРО.
В диагностике ОРО наиболее важную роль играет рентгенологический метод исследования. В большинстве случаев с помощью стандартной рентгенографии околоносовых пазух в прямой лобно-носовой или подбородочно-носовой проекциях, в вертикальном и, при наличии в пазухе гомогенного затемнения, с целью дифференцирования экссудативной формы от новообразований околоносовых пазух, в горизонтальном положениях, а также снимка черепа в косой проекции можно сделать вывод о наличии патологического процесса в околоносовых пазухах и орбите.
Необходимо отметить, что число случаев несоответствия рентгенологического заключения патологическим интраоперационным изменениями в околоносовых пазухах при ОРО колеблется от 12,5% до 27,3%.
Рентгеновская компьютерная томография значительно повысила уровень диагностики ОГС, ХГС и ОРО. Преимуществом КТ является отсутствие суммации теней вследствие мультипланарного реконструирования полученных изображений с помощью компьютера и, вследствие этого, визуальное определение пространственных взаимоотношений патологического процесса в околоносовых пазухах и прилежащих анатомических структур. Денситометрия позволяет косвенно судить о характере патологических изменений в воспалительном очаге. Как правило, КТ околоносовых пазух при ОРО проводится в коронарной и аксиальной проекциях, в исключительных случаях – в сагиттальной.
КТ используют с целью дифференциальной диагностики воспалительного отека клетчатки орбиты и ее гнойного расплавления, оценки состояния ретробульбарных структур после санации околоносовых пазух, не приведшей к улучшению клинической картины, для идентификации опухолевого или кистозного процесса, установления патологических изменений в клиновидной пазухе и в задних отделах решетчатого лабиринта.
По степени снижения воздушности околоносовых пазух определяют слабое гомогенное затемнение, интенсивное гомогенное затемнение, негомогенное затемнение, краевое снижение воздушности околоносовых пазух, горизонтальный уровень жидкости, наличие объемного образования.
В “костном” режиме на КТ определяют наличие нечеткости контуров костной стенки орбиты, наличие деструкции в виде дефектов, прерывистости контура.
В зависимости от формы ОРО отмечают различную выраженность патологических изменений в орбите. У больных с реактивным отеком век на КТ наблюдаются изменения, характерные для воспалительного процесса в пресептальной области, тогда как в постсептальном отделе повышения плотности не отмечается и, в среднем, она составляет от — 120 до — 100 HU. Острота зрения и подвижность глазного яблока не нарушаются.
Среди пациентов с отеком век и ретробульбарным отеком наиболее часто по данным КТ отмечают утолщение (отек) век, экзофтальм, повышение плотности орбиты при денситометрии до – 80 – 70 HU.
Картина орбитального целлюлита (негнойного воспаления в орбите) характеризуется утолщением век, выраженным экзофтальмом, повышением плотности до 10 – 30 HU разлитого характера и легко может быть принята за флегмону орбиты. Окончательно диагноз устанавливают во время операции, так как данным больным показано хирургическое вмешательство.
При КТ пациентов с клиническими данными субпериостального абсцесса отмечают во всех случаях наличие образования повышенной плотности (23 – 30 HU), прилежащее к той или иной стенке орбиты, отграниченное воспаленным отслоенным периостом.
Ретробульбарный абсцесс характеризуется выраженным утолщением век, резким смещением глазного яблока, наличием одного или нескольких очагов неравномерной повышенной плотности. Рентгенологическую картину дополняют изменения зрительного нерва, которые проявляются в утолщении, “размытости” контуров, нерв определяется не на всем протяжении, что указывает на его вовлечение в воспалительный процесс. Наиболее часто наблюдают локализацию абсцесса между медиальной прямой мышцей глаза и зрительным нервом.
КТ флегмоны орбиты характеризуются отчетливым разлитым неоднородным повышением плотности мягких тканей от 28 до 32 HU, смещением и деформацией глазного яблока, утолщением зрительного нерва. В околоносовых пазухах определяется содержимое с уровнем плотности, соответствующей жидкости или тотальное гомогенное снижение прозрачности, но в ряде случаев нарушений пневматизация околоносовых пазух на стороне пораженной орбиты отсутствует, что может указывать на риногенные гематогенный или лимфогенный пути инфицирования орбиты.
При всех формах ОРО на компьютерных томограммах рентгенологический диагноз гнойного воспаления в околоносовых пазухах совпадает с результатами хирургических вмешательств. Во всех случаях негнойных ОРО (реактивный отек век, реактивный отек век с интраорбитальным отеком), диагноз на компьютерной томографии может быть установлен точно, что позволяет избежать хирургического вмешательства на орбите.
По нашим данным, наиболее сложным в дифференциальной диагностике при КТ является определение гнойного характера воспаления в орбите при орбитальном целлюлите и орбитальной флегмоне. В 11,4% — 15,3% случаев на компьютерных томограммах могут быть получены признаки, напоминающие гнойное воспаление в орбите (повышение денситометрической плотности, нечеткость контуров глазных мышц, смещение глазного яблока кпереди), но окончательный диагноз может быть установлен только при вскрытии орбиты, при отсутствии гнойного отделяемого. Орбитальная клетчатка при этом отечна, цвет не светло-желтый, как в норме, а серый или с геморрагическим компонентом.
В остальных случаях гнойного воспаления в орбите (субпериостальный абсцесс, орбитальный абсцесс, орбитальная флегмона) форма гнойного воспаления согласно результатам КТ устанавливается точно, что позволяет выбрать тактику хирургического вмешательства.
При ОГС и ХГС на компьютерных томограммах локализация гнойно-воспалительного процесса в околоносовых пазухах практически совпадает с данными лечебно-диагностических пункций и результатами, полученными на операциях.
При ОРО с помощью КТ определяются различные нарушения архитектоники полости носа, способствующие возникновению и развитию воспалительного процесса в околоносовых пазухах и дальнейшему распространению его в орбиту.
По нашим данным, гипертрофия, низкое расположение решетчатой буллы, одной из важнейших составляющих остиомеатального комплекса, была выявлена по данным КТ в 29 (44,6%) случаях при орбитальных осложнениях, что было достоверно чаще, чем при остром (14 (21,5%) и хроническом (22 (33,8%) гнойных синуситах. Наряду с этим, отмечали в 36 (42,4%) случаях гипертрофию крючковидного отростка при орбитальных осложнениях. Указанная аномалия анатомии была отмечена в 19 (22,4%) случаях при остром синусите и в 30 (35,3%) при хроническом, что было достоверно меньше (p<0,01).
В большем числе наблюдений отмечена инверсия крючковидного отростка при орбитальных осложнениях (16 (50 %), чем при остром (6 (18,7%) и хроническом гнойных синуситах (30 (35,3%). Истинная гипертрофия нижней носовой раковины чаще встречалась при хроническом синусите (71 (62,3%), чем при орбитальных осложнениях (32 (28,1%). Необходимо отметить, что даже такое исследование, как КТ не всегда полностью отражает объективные изменения анатомии полости носа и окончательно определить различные патологически значимые особенности анатомии возможно только на операции. В зависимости от формы ОРО отмечали различную степень патологических изменений в орбите.
МРТ-исследование в сравнении с КТ дает меньшую информацию о характере процесса в костной ткани, что довольно важно при ОРО, ОГС и ХГС. Одной из особенностей магнитно-резонансной томографии околоносовых пазух является высокая чувствительность метода к повышенному кровенаполнению слизистой оболочки, что может привести к гипердиагностике воспалительных изменений.
Эндоскопическое исследование полости носа.
ЭИ полости носа является одним из наиболее информативных прижизненных методов исследования наряду с КТ и МРТ.
Одной из основных трудностей при проведении ЭИ полости носа является искривление перегородки носа. Данная особенность нарушения анатомии приводит, по нашим наблюдениям, к диагностике меньшего числа комбинированных деформаций перегородки носа из-за трудности осмотра задних отделов на стороне девиации перегородки носа и сужения общего носового хода. Так, у больных с ОРО отмечали комбинированное искривление перегородки носа в 20,9% случаях. При КТ комбинированные искривления перегородки носа диагностировали чаще, чем по данным ЭИ, что составило у больных с ОРО 23,9% случаев. В то же время изолированные деформации в виде гребня в указанных основных подгруппах по данным КТ были диагностированы с той же частотой, что и при ЭИ.
Большое внимание при эндоскопическом исследовании мы также уделяли размерам решетчатой воронки, крючковидного отростка, решетчатой буллы, состоянию средних и нижних носовых раковин, наличию противолежащих поверхностей, при смыкании которых, согласно H. Stammberger et al. (1990), блокируется движение ресничек мерцательного эпителия, нарушается аэрация околоносовых пазух, что приводит к застою секрета слизистой оболочки и развитию воспаления.
В 21,7% случаях при ОГС, в 33,3% при ХГС отмечали гипертрофию решетчатой буллы, что было достоверно меньше, чем при ОРО (44,9%).
Гипертрофия крючковидного отростка отмечена по данным эндоскопического исследования при ОГС и ХГС в 20,5% и 36,4% случаях, что было достоверно реже, чем при ОРО (43,2%).
Истинная гипертрофия средней носовой раковины при ОГС отмечена в 13,5% случаях, при ХГС в 32,4% случаев. В 48,6% наблюдениях отмечена указанная аномалия развития этой важнейшей составляющей остиомеатального комплекса при орбитальном осложнении.
Также, как и в случае истинной гипертрофии, буллезная деформация средней носовой раковины определена по данным эндоскопического исследования при ОРО в 44,1% случаях, что было достоверно больше, чем при ОГС (23,5%) и ХГС (32,4%).
Инверсия крючковидного отростка, сопровождающая, как правило, буллезную гипертрофию, также определена в большем числе случаев при ОРО.
Таким образом, как при КТ, так и при ЭИ носа мы отмечали в большем числе случаев наличие различных нарушений внутриносовой анатомии при ОРО, чем при ОГС и ХГС, которые отягощают его течение, в конечном итоге приводят к распространению гнойно-воспалительного процесса в орбиту.
Данные два метода являются взаимодополняющими, в частности, КТ позволяет провести оценку состояния задних отделов полости носа, недостижимых для эндоскопа вследствие выраженных нарушений со стороны перегородки носа. ЭИ имеет более высокую диагностическую ценность при определении состояния остиомеатального комплекса благодаря непосредственной визуализации комплекса в целом.
Хирургическое лечение ОРО.
Согласно современным взглядам на лечение данной патологии, санирование гнойного очага в орбите без хирургического вмешательства на околоносовых пазухах, а в ряде случаев и в полости носа не может гарантировать скорейшее выздоровление и отсутствие рецидивов в будущем.
Наиболее часто в лечении параназальных синуситов и ОРО применяются радикальные операции на околоносовых пазухах в сочетании с этмоидотомиями, широким вскрытием полости орбиты.
Большинство отечественных авторов в лечении хронических гнойных синуситов и орбитальных риносинусогенных осложнений при поражении верхнечелюстных пазух отдают предпочтение операциям по методу Колдуэлла-Люка, Иванова, Денкера, при сочетани гнойного фронтита с этмоидитом или сфеноидитом – по методу Белоголовова, Киллиана, Риделя, Янсенна – Риттера, Кунта, Янсенна – Винклера. Практически невозможно оценить преимущества или недостатки отдельных способов хирургических вмешательств, каждый из них имеет свои показания в зависимости от распространенности процесса и анатомии околоносовых пазух.
Отрицательными сторонам применения данных хирургических операций являются высокая травматичность, опасность повреждения слезного мешка, косметический дефект в виде рубца, вероятность облитерации в послеоперационном периоде носолобного соустья после радикального удаления его латеральной стенки, кратковременная диплопия в результате резекции лобного отростка вместе с блоком. Отдаленные результаты радикальных хирургических методик, оцениваемые как выздоровление, согласно данным разных авторов, наблюдаются в 50 — 80% случаев. Ведущей причиной рецидивирования хронических синуситов после операции является нарушение проходимости искусственного соустья пазухи, которое в комплексе с фиброзными послеоперационными изменениями, хроническими несанированными очагами инфекции, нарушениями внутриносовой анатомии, вызывают соприкосновение противоположных поверхностей слизистой оболочки, что приводит к поддержанию хронического воспалительного процесса и нарушению процессов репарации в оперированной пазухе.
Операции, проводимые эндоназальным доступом, отличаются отсутствием травмы мягких тканей лица и косметического дефекта. Функциональное эндоскопическое хирургическое вмешательство на околоносовых пазухах с одномоментной орбитотомией при орбитальном целлюлите и гнойных формах осложнений начинали с устранения деформации перегородки носа. С использованием КТ или МРТ определяем у пациента положение медиальной стенки орбиты в аксиальной и коронарной проекциях и определяем распространенность процесса. Одновременно во время проведения КТ и МРТ исследований дополнительно выбираем место перфорации папиросной пластинки и определяем объем вскрытия решетчатого лабиринта. Более вентральное расположение очага воспаления (верхнелатеральные, передние латеральные субпериостальные абсцессы) определяет место перфорации папиросной пластинки до уровня терминальной пластинки средней носовой раковины, вскрытие переднего отдела решетчатого лабиринта. Вовлечение в гнойно-воспалительный процесс задних отделов решетчатого лабиринта и расположение субпериостального или ретробульбарного абсцессов более дорсально обусловливает вскрытие переднего и заднего отделов решетчатого лабиринта, перфорацию медиальной стенки орбиты дорсальнее по отношению к терминальной пластинке.
Затем выполняем перфорацию медиальной стенки орбиты. Под эндоскопическим контролем проводим смещение средней носовой раковины распатором медиально, последовательно агрессивной фрезой микродебридера удаляем парциально среднюю часть крючковидного отростка, решетчатую буллу. При этом в случае локализации очага воспаления за терминальной пластинкой средней носовой раковины дополнительно вскрываем задние клетки решетчатого лабиринта и клиновидную пазуху.
Под эндоскопическим контролем перфорируем серповидным ножом папиросную пластинку в направлении сверху – вниз, спереди – назад максимально медиально по отношению к медиальной стенке орбиты. При этом обеспечиваем проникновение лезвия ножа в полость орбиты не более чем на 2 – 3 мм, длина разреза составляет 1 – 1,5 см, одномоментно с костной частью медиальной стенки вскрываем и надкостницу орбиты. Вводим в полость орбиты через рану полоску латексной резины шириной 5 мм, длиной 20 мм. Затем вводим в обе половины полости носа изогнутые в виде арки стенты из пластинчатого силикона, подогнанные индивидуально для больного, с круглым окном диаметром 1,5 см, которое прорезается в силиконе на уровне среднего носового хода, перчаточный дренаж выводим через окно в преддверие носа, далее стент фиксируем через перегородку носа одиночным узловым швом. Стенты удаляем на 3 сутки после операции.
Как правило, данное вмешательство дополняется транспальпебральной орбитотомией.
Применение ГБО в лечении ОРО.
С целью ускорения процессов репарации, уменьшения выраженности воспалительного процесса и интоксикационного синдрома больным с ОРО мы проводили на 2 – 3 сутки после операции сеансы гипербарической оксигенации.
Перед первым сеансом ГБО под эндоскопическим контролем выполняют осмотр носовых ходов и выводных отверстий соустьев околоносовых пазух с удалением при их наличии корок, с последующей анемизацией слизистой оболочки. Наряду с этим необходимо провести проверку функции слуховых труб при помощи проб Тойнби, Вальсальвы и тимпанометрии.
Первые сеансы необходимо проводить при максимальном давлении на высоте компрессии до 0,8 ата, вторые сеансы до 1,2 ата. Начиная с 3 сеанса давление в барокамере может быть повышено до 1,3 ата. Этому способствует улучшение как общего состояния больного к началу 3 сеанса, так и уменьшение выраженности воспалительных изменений в полости носа и в носоглотке, что улучшает барофункцию околоносовых пазух и проходимость слуховых труб. Продолжительность сеансов должна также подбираться индивидуально, рекомендуемая эффективная продолжительность на первом сеансе до 40 минут, в последующем до 70 минут.
С целью профилактики баротравмы всем больным перед пробными сеансами местно применяют сосудосуживающие препараты, в крайних случаях, когда у больного имеет место сопутствующий хронический экссудативный средний отит, перед ГБО проводится шунтирование барабанной перепонки больного уха.
Применение регионарной непрямой эндолимфатической терапии
в лечении орбитальных риносинусогенных осложнений.
Согласно полученным результатам экспериментального исследования, мы модифицировали методику регионарного непрямого эндолимфатического введения антибиотиков, предложенную А. Алимовым и К. Касимовым (1991). Больным с ОГС, ХГС и ОРО вводили подкожно в проекции подчелюстного лимфатического узла 8 — 12 ЕД лидазы, растворенной в 3-5 мл 0,25% раствора новокаина. Не вынимая иглы через 3 – 5 минут вводили половину разовой дозы в 2 мл физиологического раствора. Антибактериальные препараты вводили по стандартной для каждого антибиотика схеме со следующей модификацией: первую разовую дозу, например, цефотаксима, делили пополам, половину ее вводили регионарно лимфотропно, а вторую часть внутримышечно или, при орбитальных риносинусогенных осложнениях, внутривенно. Дальнейшие введения антибактериального препарата проводили по стандартной схеме с кратностью введения, указанной в рекомендациях по применению. После введения больному накладывают полуспиртовой компресс на подчелюстную область на 3 часа с целью усиления эффекта лимфостимуляции.
Рекомендуемые дозы и режимы введения антибактериальных препаратов при орбитальных риносинусогенных осложнениях.
| Антибиотики | Режимы введения |
| Цефуроксим | 0,75 регионарно лимфотропно + 0,75 в/м или в/в утром, затем по 1,5 в обед и вечером в/м или в/в. |
| Цефотаксим | 1,0 регионарно лимфотропно + 1 г в/м или в/в утром, затем по 2,0 в обед и вечером в/м или в/в. |
| Цефтриаксон | 1,0 регионарно лимфотропно + 1,0 в/м или в/в 1 раз в сутки. |
| Цефоперазон | 1,0 регионарно лимфотропно + 1 г в/м или в/в утром, затем по 2,0 в обед и вечером в/м или в/в. |
| Цефтазидим | 1,0 регионарно лимфотропно + 1 г в/м или в/в утром, затем по 2,0 в обед и вечером в/м или в/в. |
| Цефепим | 1,0 регионарно лимфотропно + 1 г в/м или в/в утром, затем по 2,0 вечером в/м или в/в. |
| Амоксициллин/клавуланат | 0,6 регионарно лимфотропно + 0,6 в/м или в/в утром, затем по 1,2 в обед и вечером в/м или в/в. |
| Имепенем | 0,25 регионарно лимфотропно и 0,25 в/м или в/в утром, далее по 0,5 х 2 раза в те же сутки в/м или в/в. |
| Меропенем | 0,25 регионарно лимфотропно и 0,25 в/м или в/в утром, далее по 0,5 х 2 раза в те же сутки в/м или в/в. |
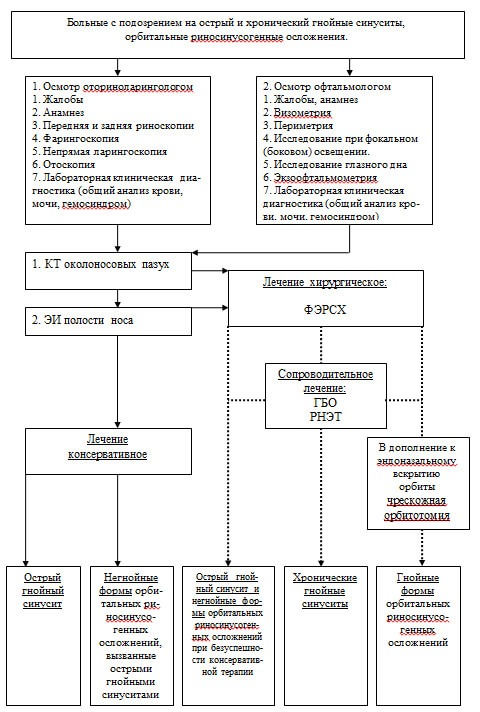
Рис.1. Лечебно-диагностический алгоритм у больных с острым и хроническим гнойными синуситами и орбитальными риносинусогенными осложнениями с использованием компьютерной томографии, функциональной эндоскопической риносинусохирургии, РНЭТ и ГБО.